Abstrak Grafis
Studi ini menggunakan elektroda MWCNT/TiO2 / TiO2 / GC yang dikembangkan untuk pertama kalinya menggunakan voltametri pulsa diferensial pelucutan adsorptif untuk menentukan daptomycin. Sensor baru, cepat, andal, hemat biaya, ramah lingkungan, sensitif, dan sangat selektif serta metode analisis yang dikembangkan membawa inovasi ke dalam literatur untuk menentukan daptomycin dalam sampel tanah, air ledeng, dan air mata air alami.
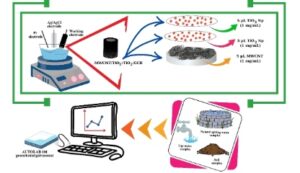
Abstrak
Daptomycin adalah antibiotik lipopeptida siklik pionir yang diperkenalkan untuk penggunaan klinis. Obat ini efektif terhadap bakteri gram positif, tetapi penggunaannya yang luas menimbulkan masalah pencemaran pada sampel lingkungan. Untuk tujuan ini, diperlukan metode analisis yang cepat, sensitif, selektif, dan dapat diterapkan untuk daptomycin dalam matriks lingkungan ini. Dalam penelitian ini, metode elektrokimia dikembangkan dengan elektroda karbon kaca (GCE) dan GCE yang dimodifikasi dari tabung nano karbon/partikel titanium dioksida/partikel titanium dioksida berdinding banyak (MWCNT/TiO 2 /TiO 2 /GCE) untuk deteksi daptomycin menggunakan voltametri pulsa diferensial pelepasan adsorptif. Karakterisasi permukaan sensor yang didukung diteliti. Dalam kondisi yang dioptimalkan, rentang linier untuk elektroda yang tidak dimodifikasi dan MWCNT/TiO2 / TiO2 / GCE adalah 0,2–1,0 μM dan 0,06–5,0 μM, dengan batas deteksi 0,086 μM dan 0,001 μM. Selektivitas sensor yang diusulkan diselidiki untuk senyawa organik dan anorganik yang dapat memengaruhi deteksi daptomycin melalui studi interferensi. Keakuratan metode yang diusulkan untuk menentukan daptomycin dalam berbagai sampel lingkungan (tanah, mata air alami, dan air ledeng) dihitung sebagai % pemulihan dalam studi pemulihan. Sensor yang baru, cepat, andal, hemat biaya, ramah lingkungan, sensitif, dan sangat selektif dikembangkan untuk pertama kalinya guna menentukan daptomycin dalam sampel lingkungan, yang memperkenalkan metode analitis baru ke dalam literatur.
1 Pendahuluan
Daptomycin adalah antibiotik lipopeptida siklik yang diproduksi melalui fermentasi Streptomyces roseosporous (Skema S1). 1 Antibiotik ini menghambat bakteri Gram-positif dan telah tersedia untuk penggunaan klinis sejak tahun 2001. Cara kerja daptomycin melibatkan depolarisasi membran sel bakteri, yang menyebabkan kematian bakteri secara cepat karena penghambatan sintesis DNA, RNA, dan protein. Yang lebih penting, daptomycin telah menunjukkan aktivitas yang kuat terhadap Staphylococcus aureus yang resistan terhadap methicillin (MRSA) dan enterococci yang resistan terhadap vankomisin. Selain itu, daptomycin telah diidentifikasi sebagai agen antimikroba yang potensial untuk mengobati infeksi S. aureus pada hewan liar dan ternak, termasuk hewan peliharaan, spesies hewan produksi, dan satwa liar. Namun, nilai konsentrasi penghambatan minimal (MIC) dapat bervariasi tergantung pada spesies hewan, lokasi infeksi, dan pengalaman klinis. Meskipun secara diagnostik sulit dan berpotensi kompetitif, pupuk kandang kini diakui sebagai sumber potensial penularan MRSA pada manusia, dan daptomycin telah menjadi pilihan yang menjanjikan untuk mengendalikan infeksi S. aureus multiresisten yang serius dan infeksi MRSA dengan satu strategi kesehatan. 2
Bahasa Indonesia: Ketika penelitian yang dilakukan sejauh ini diperiksa, terlihat bahwa metode analisis tradisional seperti kromatografi, kromatografi cair 3 – 5 yang digabungkan dengan spektrometri massa tandem, 6 – 9 dan spektrofotometri 10 , 11 digunakan secara luas untuk penentuan daptomycin. Metode tradisional memiliki kelemahan seperti memerlukan perangkat yang mahal, langkah pra-perlakuan yang rumit, waktu analisis yang lama, penggunaan pelarut organik dalam jumlah tinggi, dan produksi limbah yang tinggi. Karena alasan ini, metode elektrokimia telah mendapatkan popularitas dalam beberapa tahun terakhir karena sifat-sifatnya yang unggul. Metode elektrokimia memiliki beberapa keunggulan, seperti analisis cepat, rentang aplikasi yang luas, deteksi analit pada konsentrasi rendah, tidak memerlukan pra-perlakuan, konsumsi pelarut organik rendah, dan studi waktu nyata. 12 – 14 Penggunaan metode elektroanalisis dalam penentuan senyawa farmasi, termasuk antibiotik, telah dilaporkan dalam banyak penelitian sebelumnya. 15 – 18 Elektroda karbon kaca (GCE) telah mendapatkan perhatian dalam berbagai aplikasi teknologi karena sifat kimia, mekanik, listrik, dan termalnya yang sangat baik. Mereka telah digunakan dalam sensor elektrokimia untuk deteksi molekuler, sistem penyimpanan energi, dan perangkat pengolahan air limbah. 19 Lebih jauh lagi, GCE menawarkan beberapa keuntungan dalam analisis voltametri. Mereka juga menunjukkan karakteristik semimikroelektroda, yang dapat meningkatkan rasio sinyal terhadap derau dan memungkinkan pengukuran dalam larutan resistif tinggi. 20 Lebih jauh lagi, GCE yang tidak dimodifikasi dapat digunakan untuk penginderaan pH karena adanya gugus kuinon pada permukaannya, yang menunjukkan respons Nernstian pada rentang pH yang luas. 21 GCE menunjukkan penyerapan senyawa organik yang lebih baik, khususnya aromatik, dibandingkan dengan elektroda karbon lainnya, yang meningkatkan kinerjanya dalam voltametri pelucutan adsorptif. 22 Karena sifat elektroda GC yang unggul, elektroda ini dipilih sebagai elektroda kerja dalam penelitian ini.
Itaya dan Bard menerbitkan laporan awal tentang modifikasi permukaan elektroda untuk persiapan dan desain sensor elektrokimia pada tahun 1978. 23 Selanjutnya, banyak penelitian telah dilakukan untuk merancang dan mengembangkan sensor elektrokimia di berbagai domain aplikasi. Sensor elektrokimia selektif dan sensitif yang cocok untuk menganalisis zat dapat dikembangkan menggunakan banyak elektroda berbeda dan berbagai bahan modifikasi. 24 – 26 Menggunakan nanomaterial sebagai bahan modifikasi adalah pilihan umum untuk meningkatkan kinerja sensor elektrokimia, terutama dalam hal sensitivitas. Meningkatkan sifat konduktif dan listrik sensor berbasis nanomaterial ini memungkinkan percepatan kinetika transfer elektron dan peningkatan respons sinyal. Nanotube karbon berdinding banyak (MWCNT) menawarkan keuntungan signifikan dalam deteksi voltametri berbagai analit. Elektroda yang dimodifikasi MWCNT meningkatkan sensitivitas dan memberikan batas deteksi yang lebih rendah dibandingkan dengan elektroda konvensional. 27 , 28 Elektroda berbasis MWCNT menawarkan keuntungan seperti penanganan mudah, ketahanan terhadap pengotoran permukaan, dan biaya rendah. 27 Aplikasinya berkisar dari analisis farmasi hingga pemantauan lingkungan terhadap berbagai kontaminan dalam sampel air. Nanopartikel TiO2 menawarkan keuntungan signifikan dalam voltametri dan aplikasi penginderaan elektrokimia. Dimensi skala nanonya meningkatkan kapasitas penyimpanan muatan melalui proses interkalasi dan pseudokapasitif, dengan partikel di bawah 10 nm menunjukkan peningkatan kontribusi kapasitif. 29 Sifat fotokatalitik nanopartikel TiO2 semakin memperluas potensi aplikasinya dalam remediasi lingkungan dan produksi energi, meskipun ada keterbatasan seperti penyerapan cahaya tampak yang buruk. 30 Secara keseluruhan, nanopartikel TiO2 meningkatkan kinerja elektrokimia dan menawarkan fleksibilitas dalam aplikasi penginderaan dan katalitik.
Studi terkini telah mengeksplorasi berbagai metode elektrokimia untuk mendeteksi daptomycin, antibiotik lipopeptida siklik (Tabel S1). Rabiee dkk. (2020) mengembangkan teknik sensitif yang menggabungkan ekstraksi elektro-membran dan voltametri siklik kontinu, yang mencapai batas deteksi 3,5 ng/mL. 31 Ozcelikay dkk. (2020) menciptakan sensor polimer bercetakan molekuler menggunakan nanopartikel platinum berhias emas, yang mencapai batas deteksi 0,161 pM. 32 Machini & Oliveira-Brett (2017) menyelidiki perilaku redoks daptomycin pada elektroda karbon kaca, yang menentukan oksidasinya sebagai proses ireversibel dua langkah dengan batas deteksi 0,32 μM. 33 Aslan dkk. (2024) menyelidiki interaksi daptomycin-DNA dengan elektroda grafit pensil sekali pakai. Interaksi DAP dengan DNA diteliti menggunakan teknik voltametri, spektrofotometri, dan docking molekuler. Batas deteksi ditetapkan sebesar 0,032 mg/mL dengan metode ini. 34 Metode elektrokimia ini menawarkan alat deteksi dan kuantifikasi daptomycin yang menjanjikan dalam berbagai matriks, termasuk cairan biologis. Ben Jaballah dkk. (2022) mengembangkan sensor untuk mendeteksi daptomycin dalam sampel air mineral dan air ledeng menggunakan elektroda karbon cetak saring (SPCE) yang dimodifikasi dengan nanopartikel tembaga sintetis hijau (CuNPs) menggunakan ekstrak tanaman Moringa oleifera . Batas deteksi (LOD) deteksi daptomycin ditetapkan sebesar 0,01 g/L. 35 Ketika penelitian yang dilakukan diperiksa, terlihat bahwa tidak ada penelitian sebelumnya untuk penentuan daptomycin dalam tanah, mata air, dan air ledeng. Oleh karena itu, bertujuan untuk mengisi kesenjangan ini dalam literatur dengan mengembangkan sensor dan metode baru.
Dalam lingkup penelitian ini, sensor voltametri yang lebih cepat, lebih selektif, sensitif, presisi, dan sangat berulang dikembangkan daripada sensor elektrokimia yang dilaporkan dalam literatur menggunakan elektroda karbon kaca yang dimodifikasi dengan nanomaterial untuk daptomycin. Karakterisasi permukaan sensor yang dikembangkan dilakukan dengan mikroskop elektron pemindaian (SEM) dan detektor sinar-X dispersif energi mikroskop elektron pemindaian (SEM-EDX). Luas permukaan sensor yang dikembangkan dihitung menggunakan teknik voltametri siklik (CV). Optimasi metode dan studi rentang linier dilakukan dengan AdSDPV dalam lingkungan yang sesuai untuk sensor yang diusulkan. Aplikasi analitis pertama dari nanosensor yang disarankan dilakukan untuk mendeteksi daptomycin dalam air ledeng, air mata air alami, dan sampel tanah. Orisinalitas penelitian ini dibuktikan dengan fakta bahwa sensor yang dikembangkan untuk daptomycin digunakan untuk pertama kalinya dalam literatur, nilai batas deteksi (LOD) dan batas kuantifikasi (LOQ) yang diperoleh lebih rendah daripada LOD dan LOQ yang lebih rendah yang ditetapkan dalam literatur, dan aplikasi elektrokimia zat-zat ini dalam sampel tanah, air mata air alami, dan air keran adalah yang pertama kalinya. Hasilnya, sensor yang dapat diulang, sensitif, selektif, dapat diterapkan, dan ramah lingkungan telah dikembangkan untuk mendiagnosis daptomycin dalam penelitian ini.
Bagian Eksperimen
Bahan Kimia dan Peralatan
Semua reagen yang digunakan dalam penelitian ini bermutu analitis dan digunakan tanpa pemurnian lebih lanjut. Daptomycin bersumber dari VEM Pharmaceuticals AS (İstanbul, Türkiye). Zat-zat berikut juga diperoleh dari Sigma-Aldrich (Darmstadt, Jerman): etanol, N, N-dimetilformamida (DMF), asam asetat glasial (CH3COOH , >99 %), asam fosfat (H3PO4 , > 85 %), asam sulfat ( H2SO4 , 96–98 %), asam borat (H3BO3 , > 99 %), natrium hidroksida (NaOH, >97 %), asam klorida (HCl , 37 %), kalium klorida (KCl), natrium klorida (NaCl), natrium bikarbonat (NaHCO3 ) , magnesium nitrat (Mg(NO3 ) 2 ) , parasetamol, dan pirfenidone. Nanotube karbon berdinding ganda (MWCNT) juga dibeli dari Sigma-Aldrich (Darmstadt, Jerman), sedangkan TiO 2 Np (nanopartikel titanium dioksida, 17 nm) diperoleh dari Nanografi (Ankara, Türkiye).
Data elektrokimia diperoleh menggunakan penganalisa potensiostat/galvanostat (AUTOLAB101, Metrohm AG, Swiss) dengan sel tiga elektroda voltametri. Elektroda lawan dipilih sebagai kawat platina (Pt) (MW-1032). Elektroda referensi adalah Ag/AgCl (3 M NaCl, MF-2052), dan elektroda kerja dipilih sebagai elektroda karbon kaca (2012, diameter ϕ=3 mm). Semua elektroda yang digunakan tersedia dalam merek BASi ® (West Lafayette, AS). Teknik voltametri, termasuk voltametri pulsa diferensial (DPV), voltametri pulsa diferensial pelepasan adsorptif (AdSDPV), dan voltametri siklik (CV), digunakan untuk melakukan eksperimen elektrokimia. Pengukur pH portabel (ISOLAB, Jerman) digunakan untuk pengukuran pH, dan neraca elektronik (presisi ±0,0001 g) (Shimadzu, ATX224R, Kyoto, Jepang) digunakan untuk menimbang bahan kimia secara tepat. Bak ultrasonik (ISOLAB, Jerman) digunakan untuk memastikan persiapan sampel yang homogen. Penganalisis Zeiss EVO 50 (Merlin, Carl Zeiss, Oberkochen, Jerman) digunakan untuk memperoleh spektrum EDX dan gambar SEM.
Mempersiapkan Solusi Standar
Persiapan larutan standar DPT 0,1 mM melibatkan pelarutan zat dalam air suling. Larutan stok diencerkan dengan asam sulfat (0,5 M–0,1 M)) elektrolit pendukung dan larutan buffer yang berbeda (Britton–Robinson (BRB, pH 2,0–12,0), asetat (ABS, pH 3,7–4,7–5,7), dan fosfat (PBS, pH 1,5–8,0)), untuk menghasilkan konsentrasi larutan standar yang berbeda untuk semua pengukuran. Zat anorganik (CuSO4 , Mg(NO3 ) 2 , KCl, NaHCO3 ) dan senyawa organik parasetamol digunakan dalam studi interferensi dan disiapkan menggunakan air murni. Senyawa organik seperti larutan pirfenidone tersedia dalam etanol. Semua larutan disimpan dalam lemari es (+4 °C).
Persiapan Sampel Tanah dan Air yang Berbeda
Sampel air keran DPT 0,1 mM dan air mata air alami disiapkan secara terpisah dengan menambahkan larutan stok DPT 1 mM (1 mL) dan sampel air (9 mL). Sampel tanah yang mengandung DPT 1 mM disiapkan dalam volume 50 mL dengan menimbang 1 g sampel tanah dan jumlah DPT yang dibutuhkan, lalu mencampurnya. Setelah didiamkan dalam bak ultrasonik selama 20 menit, sampel disaring dengan kertas saring. Semua sampel diencerkan dari stok induk dan digunakan dalam studi akurasi dan pemulihan.
Persiapan Elektroda MWCNT/TiO2 / TiO2 / GC yang dimodifikasi
Sebelum analisis, GCE polos dimurnikan dengan etanol dan air suling (1 : 1, v/v) dalam bak ultrasonik selama lima menit. Setelah itu, aktivasi dilakukan dengan 10 siklus CV. Setelah pengukuran, permukaan elektroda polos dicuci dengan air murni, dipoles dengan bubur alumina polikristalin, dibersihkan dengan hati-hati menggunakan air murni, dan dikeringkan pada suhu kamar. Kemudian, campuran MWCNT (1 mg/mL) (5 μL) diteteskan ke GCE polos sebagai lapisan pertama dan dikeringkan pada suhu 50 °C dalam vakum selama 15 menit. Kemudian, 5 μL suspensi TiO2 ( 1 mg/mL) diteteskan ke permukaan elektroda yang dilapisi dan dikeringkan (50 °C, 10 menit). Setelah permukaan elektroda kering, 5 μL suspensi TiO2 ( 1 mg/mL) diteteskan sebagai lapisan ketiga dan dikeringkan (50 °C, 10 menit). Dengan demikian, elektroda yang dimodifikasi disiapkan. Hasilnya, permukaan sensor tiga lapis dikembangkan.
2 Hasil dan Pembahasan
2.1 Karakterisasi Elektroda Modifikasi MWCNT/ TiO2 / TiO2
Karakterisasi permukaan sensor yang didukung dianalisis menggunakan SEM dan SEM-EDX. Luas permukaan sensor yang dikembangkan dalam larutan Fe 3+ /Fe 4+ dihitung menggunakan voltametri siklik. Hasilnya, terbukti bahwa luas permukaan GCE meningkat sekitar dua kali lipat dengan sensor yang dikembangkan dengan menghitungnya dengan persamaan Randles-Sevcik pada pembacaan arus ferri/ferro dengan CV. Terlihat juga dengan gambar SEM dan SEM-EDX bahwa permukaannya ditutupi dengan MWCNT dan nanomaterial TiO 2 .
Untuk meneliti karakteristik morfologi permukaan elektroda yang dilapisi dengan MWCNT/TiO 2 /TiO 2 , permukaan elektroda diperiksa dengan SEM dan EDX. Karakterisasi permukaan (A) elektroda yang tidak dimodifikasi, (B) MWCNTs, (C) TiO 2 NPs, (D) MWCNT/TiO 2 NPs, dan (E) MWCNT/TiO 2 /TiO 2 diperoleh dengan SEM pada skala batang 200 nM, dan spektrum EDX dari MWCNT/TiO 2 /TiO 2 (F) diperoleh dengan SEM-EDX (Gambar 1 ). Morfologi GCE murni memiliki permukaan yang licin dan hitam (Gambar 1A ). Seperti yang ditunjukkan pada Gambar 1B , MWCNT memiliki struktur filamen. TiO 2 NPs hampir berbentuk bulat (Gambar 1C ). Ketika morfologi permukaan MWCNT/TiO2 diperiksa , terlihat bahwa ada lapisan TiO2 NP pada filamen MWCNT (Gambar 1D ). Sementara morfologi permukaan MWCNT/TiO2 / TiO2 diselidiki pada Gambar 1E , terlihat bahwa TiO2 NP dilapisi dalam dua lapisan pada filamen MWCNT, dan luas permukaan elektroda diperbesar. Dengan demikian, secara visual terbukti bahwa luas permukaan elektroaktif elektroda telanjang meningkat dengan pengubah MWCNT/TiO2 / TiO2 . Seperti yang ditunjukkan pada Gambar 1F , spektrum EDX memverifikasi bahwa TiO2 hadir pada permukaan elektroda.

Gambar 1
Buka di penampil gambar
Kekuatan Gambar
Gambar SEM dari GCE (A) yang tidak dimodifikasi, MWCNTs (B), TiO 2 Np (C), MWCNT/TiO 2 (D) dan MWCNT/TiO 2 /TiO 2 (E), spektrum EDX dari MWCNT/TiO 2 /TiO 2 (F).
Untuk menilai sifat permukaan dan kinerja analitis elektroda termodifikasi MWCNT/TiO2/TiO2 yang disiapkan untuk DPT , voltamogram siklik diperoleh dalam larutan Fe3 + /Fe4 + . Sensor yang dikembangkan dan elektroda polos dilawan dengan mengambil arus puncak larutan Fe3 + /Fe4 + yang terbentuk pada laju pemindaian 100 mV s −1 antara +1,2 V dan −0,6 V dengan CV dalam 0,1 M KCl dalam larutan Fe3 + /Fe4 + 5,0 mM (Gambar S1).
Luas permukaan elektroaktif sensor MWCNT/TiO2 / TiO2 dihitung menggunakan persamaan Randles-Sevcik (Ip=2,69×105 n3/ 2ACD1 / 2v1 / 2 ). A menyatakan luas permukaan elektroaktif, C menyatakan konsentrasi larutan ferri/ferro, D menyatakan koefisien difusi larutan ferri/ferro, Ip menyatakan arus puncak, laju pemindaian v , dan n menyatakan jumlah transfer elektron. Luas permukaan elektroaktif elektroda GCE yang tidak dimodifikasi dan elektroda MWCNT/TiO2 / TiO2 yang dimodifikasi masing-masing adalah 0,065 dan 0,153 cm2 . Hasilnya, terbukti bahwa elektroda yang dimodifikasi dengan MWCNT/TiO2 / TiO2 memiliki luas permukaan elektroaktif sekitar 2 kali lebih besar daripada GCE yang tidak dimodifikasi.
2.2 Konduktivitas Elektrokimia DPT pada MWCNT/TiO2 / TiO2 / GCE
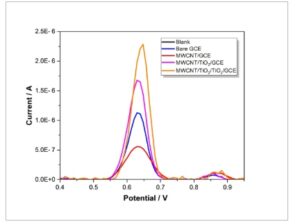
Sinyal anoda DPT 0,005 mM direkam oleh AdSDPV dengan GCE polos, MWCNT, MWCNT/TiO2 dan GCE yang dimodifikasi MWCNT/TiO2/TiO2 (Gambar 2 ) . Ketika sinyal yang diperoleh oleh AdSDPV dibandingkan, modifikasi tersebut menunjukkan efek yang signifikan pada proses elektrooksidasi. Arus oksidasi DPT pada MWCNT/TiO2 / TiO2 / GCE sekitar 5,5 kali lebih tinggi daripada GCE polos.
Gambar 2
Buka di penampil gambar
Kekuatan Gambar
Voltamogram diperoleh dengan AdSDPV menggunakan GCE yang tidak dimodifikasi dan elektroda yang dimodifikasi dalam buffer fosfat pH 7,5 untuk penentuan 0,005 mM DPT (parameter AdSDPV: langkah E: 9 mV, waktu pulsa: 50 ms, amplitudo pulsa: 60 mV, waktu interval: 0,5 dtk, Eacc: 0 V, tacc: 60 dtk).
Pada Gambar S2 terlihat bahwa sinyal daptomycin meningkat 5,5 kali lipat seiring dengan peningkatan luas permukaan elektroda yang terbentuk dengan membentuk dua lapisan TiO2 pada permukaan GCE yang dilapisi MWCNT dan terjadi penurunan respons sinyal ketika 10 mikroliter TiO2 langsung diteteskan. Terbukti bahwa sensor yang dibuat dengan melapisi dua lapisan TiO2 pada MWCNT merupakan elektroda yang lebih sensitif dengan sinyal yang tinggi. Penelitian eksperimental dilanjutkan dengan menggunakan sensor MWCNT/TiO2 / TiO2 / GCE.
2.3 Pengaruh pH terhadap Penentuan DPT
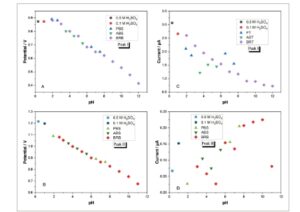
Efek pH elektrolit pendukung pada oksidasi DPT diteliti dalam pH yang berbeda (0,3–12,0) dengan elektrolit pendukung H2SO4 ( 0,1 M dan 0,5 M) , larutan AB, PB dan BRB dan menggunakan teknik DPV. Efek pH pada Ip dan Ep anoda untuk DPT 0,1 M dievaluasi untuk GCE polos. Ini menunjukkan sinyal anoda tertinggi dalam medium elektrolit pendukung 0,5 MH2SO4 dengan elektroda polos (Gambar 3C ) . Terlihat pada Gambar 3A dan 3B bahwa nilai Ep DPT menurun dengan meningkatnya nilai pH. Karena respons puncak II berada pada nilai yang sangat kecil, analisis dievaluasi berdasarkan puncak I. Untuk alasan ini, penelitian dilanjutkan dalam medium 0,5 MH2SO4 menggunakan elektroda polos .
Gambar 3
Buka di penampil gambar
Kekuatan Gambar
Hasil yang diperoleh dengan DPV menggunakan GCE kosong untuk DPT 0,1 mM dalam larutan elektrolit pendukung dengan nilai pH berbeda: A) Grafik pH-Potensial Puncak I, B) Grafik pH-Potensial Puncak II, C) Grafik pH-Arus Puncak I, D) Grafik pH-Arus Puncak II (Parameter AdSDPV: langkah E: 9 mV, waktu pulsa: 50 ms, amplitudo pulsa: 60 mV, waktu interval: 0,5 d).
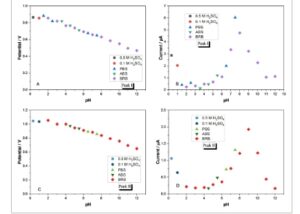
Dampak pH pada Ip dan Ep untuk DPT 0,05 M dinilai dengan MWCNT/TiO2 / TiO2 / GCE. Terlihat pada Gambar 4B bahwa respons tertinggi diperoleh untuk Puncak I dengan sensor yang dikembangkan pada pH 7,5 PBS. Terlihat pada Gambar 4D bahwa sinyal tertinggi untuk Puncak II berada pada pH 9,0 BRB. Terlihat pada Gambar 4A dan 4C bahwa nilai Ep DPT menurun dengan meningkatnya nilai pH. Diperkirakan bahwa Puncak II memberikan sinyal yang lebih rendah daripada Puncak I, yang akan membuat analisis lebih sulit pada konsentrasi yang lebih rendah. Oleh karena itu, penelitian dilanjutkan dalam media PBS pH 7,5 menggunakan MWCNT/TiO2 / TiO2 / GCE.
Gambar 4
Buka di penampil gambar
Kekuatan Gambar
Hasil yang diperoleh dengan MWCNT/TiO2 / TiO2 / GCE dan 0,1 mM DPT dan DPV dalam larutan elektrolit pendukung dengan nilai pH yang berbeda. A) Grafik pH-Potensial Puncak I. B) Grafik pH-Arus Puncak I. C) Grafik pH-Potensial Puncak II. D) Grafik pH-Arus Puncak II (parameter AdSDPV: langkah E: 9 mV, waktu pulsa: 50 ms, amplitudo pulsa: 60 mV, waktu interval: 0,5 d).
2.4 Pengaruh Kecepatan Pemindaian terhadap Penentuan DPT
Studi laju pemindaian ( v ) dilakukan untuk menjelaskan mekanisme oksidasi elektrokimia DPT pada permukaan yang tidak dimodifikasi dan MWCNT/TiO 2 /TiO 2 /GCE. Efek laju pemindaian yang berbeda (50–1000 mV s −1 ) untuk GCE polos pada nilai Ip DPT 1 mM dalam larutan pendukung 0,5 MH 2 SO 4 diselidiki oleh CV (Gambar S3). Saat laju pemindaian meningkat, Ip meningkat, dan Ep bergeser ke nilai yang lebih positif. Peningkatan potensial sinyal pada laju pemindaian yang lebih tinggi menunjukkan proses transfer elektron yang ireversibel. Lebih jauh lagi, sinyal yang jelas dicatat pada puncak oksidasi, sementara tidak ada sinyal balik yang sesuai muncul untuk sinyal anoda dalam pemindaian katoda. Ini menunjukkan bahwa DPT mengalami reaksi ireversibel pada elektroda.
Persamaan yang diperoleh dengan CV dengan DPT 1 mM dalam larutan 0,5 MH 2 SO 4 dengan GCE polos adalah sebagai berikut:
log Ip (μA) = 0,7563 log v (mVs −1 ) – 0,9703 (r = 0,9973, n = 7)
Nilai Ip (μA) = 0,7263 v 1/2 (mVs −1 ) – 3,7106 (r = 0,9926, n = 7)
Nilai Ip (μA) = 0,0189 v (mVs −1 ) + 1,6943 (r = 0,9885, n = 7)
Kemiringan grafik log v versus dan log Ip yang diperoleh dengan logaritma laju pemindaian dan logaritma arus puncak digunakan untuk menginterpretasikan mekanisme transfer elektron DPT. Kemiringan grafik yang mendekati 1 menunjukkan proses yang dikendalikan oleh adsorpsi, sedangkan kemiringan 0,5 menunjukkan proses yang dikendalikan oleh difusi. 36 – 38 Nilai kemiringan persamaan linier antara log Ip dan log v untuk sensor yang dikembangkan dihitung sebesar 0,79. Nilai ini membuktikan bahwa mekanisme transfer elektron pada permukaan GCE polos dalam larutan MH 2 SO 4 0,5 dari perilaku elektrokimia DPT dikendalikan oleh difusi dalam adsorpsi.
Dampak laju pemindaian yang berbeda dengan arus anoda DPT 0,1 mM untuk sensor MWCNT/TiO2 / TiO2 / GCE diselidiki dengan voltametri siklik (Gambar S4). Buffer fosfat pH 7,5 dipilih sebagai media yang cocok untuk pemindaian kecepatan, di mana sinyal tertinggi diperoleh untuk puncak I dan II. Diamati bahwa arus oksidasi meningkat dan potensial anoda bergeser ke nilai yang lebih positif dengan meningkatnya laju pemindaian antara 25 dan 1000 mV s−1 dalam media PBS pH 7,5. Sinyal puncak II tidak diamati pada kecepatan pemindaian lebih rendah dari 100 mV s −1 . Evaluasi dilakukan antara nilai 100 dan 1000 mV s −1 untuk puncak II. Sementara sinyal yang jelas diamati selama pemindaian anoda, tidak ada sinyal yang sesuai yang terdeteksi untuk potensial oksidasi dalam pemindaian katoda. Peningkatan potensial sinyal dengan laju pemindaian menunjukkan mekanisme transfer elektron yang ireversibel. Hal ini menunjukkan bahwa DPT mengalami reaksi elektroda yang ireversibel.
Persamaan yang diperoleh dengan CV dengan 0,1 mM DPT dalam medium PBS pH 7,5 dengan sensor MWCNT/TiO2 /TiO2 /GCE yang dikembangkan adalah sebagai berikut :
Untuk Puncak I;
logaritma Ip (μA) = 0,7983 logaritma v (mVs −1 ) – 1,02 (r = 0,9887, n = 8)
Nilai Ip (μA) = 0,0265 v (mVs −1 ) + 0,5294 (r = 0,9699, n = 8)
Nilai Ip (μA) = 0,9407 v 1/2 (mVs −1 ) – 5,4024 (r = 0,9386, n = 8)
Untuk Puncak II;
log Ip (μA) = 1,2371 log v (mVs −1 ) – 2,7835 (r = 0,9893, n = 5)
Nilai Ip (mV) = 0,0079 v (mVs -1 ) – 0,175 (r = 0,9908, n = 5)
Nilai Ip (μA) = 0,3282 v 1/2 (mVs −1 ) – 3,1268 (r = 0,9863, n = 5)
Nilai kemiringan grafik log v versus log Ip untuk sensor yang dikembangkan dihitung sekitar 0,7983 dan 1,237 untuk puncak I dan puncak II dalam medium PBS pH 7,5. Nilai ini membuktikan bahwa proses transfer elektron dari perilaku elektrokimia DPT pada permukaan sensor yang dikembangkan dikontrol oleh difusi di bawah adsorpsi untuk puncak I dan dikontrol oleh adsorpsi untuk puncak II.
Persamaan Laviron (mathematical equation mathematical equation mathematical equation mathematical equation mathematical equation mathematical equation ) digunakan untuk menghitung jumlah elektron yang berpartisipasi dalam reaksi elektrokimia. F adalah konstanta Faraday (96485 C mol −1 ), T adalah suhu (298 K), R adalah konstanta gas (8,314 J K mol −1 ), n adalah jumlah elektron, dan α adalah koefisien transfer elektron. Jumlah elektron yang berpartisipasi dalam reaksi dihitung menggunakan persamaan Laviron menurut persamaan log v – Ep berikut. Dengan menggunakan persamaan Laviron, jumlah elektron adalah 2,74 dan 1,95 untuk elektroda yang tidak dimodifikasi dan dimodifikasi.
Ep (V)=0,0431 log v (Vs −1 )+1,0443 (r=0,9916, n=7) untuk elektroda telanjang dalam larutan 0,5 MH 2 SO 4
Ep (V) = 0,06005 log v (Vs −1 ) + 0,7765 (r = 0,9901, n = 7) untuk elektroda yang dimodifikasi dalam larutan pH 7,5
2.5 Optimasi Kondisi Eksperimen
Teknik AdSDPV digunakan dengan elektroda polos dan termodifikasi untuk menentukan DPT. Parameter teknik DPV, langkah E, waktu pulsa, amplitudo pulsa, dan waktu interval dioptimalkan untuk DPT 0,05 mM dalam medium PBS pH 7,5 dengan elektroda termodifikasi MWCNT/TiO2 /TiO2 . Efek waktu pulsa pada penentuan DPT diselidiki dalam rentang 30–70 ms. Sinyal anoda meningkat secara linear hingga 50 ms dan menurun setelah 60 ms (Gambar S5A). Waktu pulsa optimal ditentukan menjadi 50 ms, di mana arus tertinggi yang dapat direproduksi direkam. Efek langkah E pada penentuan DPT diselidiki antara 7–11 mV. Arus meningkat secara linear dari 7 mV–9 mV. Penurunan arus yang signifikan diamati setelah 9 mV (Gambar S5B). Langkah E dipilih sebagai 9 mV, di mana arus tertinggi diperoleh. Efek amplitudo pulsa pada sensor yang dikembangkan diselidiki antara 20–120 mV untuk DPT. Sinyal meningkat secara linear antara 20–80 mV. Arus puncak menurun secara linear dari 100 mV. Amplitudo pulsa ditetapkan ke 80 mV, dan sinyal tertinggi diperoleh (Gambar S5C). Dampak waktu interval untuk deteksi DPT dievaluasi antara 0,3–0,8 detik. Sementara peningkatan linear diamati dalam kisaran 0,3–0,5 detik, penurunan linear diamati setelah 0,5 detik. Waktu interval optimum 0,5 detik dipilih (Gambar S5D).
Studi laju pemindaian menunjukkan bahwa reaksi oksidasi elektrokimia DPT dikontrol oleh difusi di bawah adsorpsi dengan MWCNT/TiO2 / TiO2 / GCE. Menggunakan parameter DPV yang dioptimalkan, waktu akumulasi (t acc ) dan potensial akumulasi (E acc ) dioptimalkan. Eksperimen dilakukan pada 0,006 mM DPT dalam medium PBS pH 7,5. Efek potensial akumulasi pada sinyal DPT diteliti antara -0,1 V dan 0,3 V. Sinyal anoda DPT diikuti secara bertahap dengan potensial akumulasi bervariasi antara -0,1 dan 0,3 V, menjaga waktu akumulasi konstan pada 30 detik (Gambar S6a). Untuk optimalisasi waktu akumulasi, potensial akumulasi 0,0 V dipilih, di mana sinyal DPT adalah yang tertinggi. Dampak waktu akumulasi pada sinyal anoda DPT diselidiki dalam rentang 0–180 detik. Arus puncak naik selama 150 detik sebelum menurun (Gambar S6b). Percobaan dilanjutkan dengan menjaga E acc optimum pada 0,0 V dan t acc konstan pada 150 detik.
Studi sensitivitas untuk elektroda polos dan termodifikasi dilakukan menggunakan parameter yang sama untuk metode yang dikembangkan.
2.6 Kinerja Analisis Elektroda Telanjang dan Elektroda Termodifikasi
Investigasi komprehensif dilakukan terkait linearitas, yang dianggap sebagai salah satu parameter validasi untuk menentukan DPT menggunakan metode elektrokimia yang diusulkan. Studi ini mengevaluasi kinerja voltametri GCE yang tidak dimodifikasi dan MWCNT/TiO2 / TiO2 / GCE untuk menentukan DPT pada berbagai konsentrasi DPT menggunakan AdSDPV yang dioptimalkan. 3 dan 10 kali nilai yang diperoleh dengan membagi deviasi standar (SD) dari konsentrasi analit terendah dalam rentang linear yang ditentukan oleh metode dengan kemiringan (m) kurva kalibrasi dinyatakan sebagai LOD dan LOQ, masing-masing.
Voltammogram diperoleh dengan AdSDPV dalam medium elektrolit pendukung 0,5 MH 2 SO 4 yang mengandung berbagai konsentrasi DPT (Gambar 5A ) menggunakan elektroda yang tidak dimodifikasi. Seperti yang ditunjukkan pada Gambar 5B , kurva linier diperoleh dalam kisaran 0,2–1,0 μM. LOD dan LOQ dihitung masing-masing sebesar 0,086 dan 0,286 μM untuk GCE murni menggunakan grafik kalibrasi.
Gambar 5
Buka di penampil gambar
Kekuatan Gambar
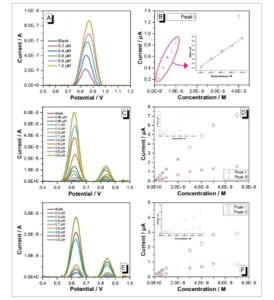
Voltammogram AdSDP dan grafik kalibrasi pada GCE polos dalam 0,5 MH 2 SO 4 (A,B); sensor MWCNT/TiO 2 /TiO 2 dalam PBS pH 7,5 (C,F); sampel tanah yang dicampur DPT dengan MWCNT/TiO 2 /TiO 2 /GCE dalam PBS pH 7,5 (E,F) dengan berbagai konsentrasi DPT (parameter AdSDPV: langkah E: 9 mV, waktu pulsa: 50 ms, amplitudo pulsa: 80 mV, waktu interval: 0,5 d, Eacc: 0 V, tacc: 150 d).
Studi linearitas dilakukan untuk mendeteksi berbagai konsentrasi DPT dalam medium fosfat pH 7,5 dengan AdSDPV menggunakan MWCNT/TiO2 / TiO2 / GCE. Voltamogram yang diperoleh ditunjukkan pada Gambar 5C . Arus menunjukkan hubungan linear terhadap konsentrasi DPT dalam medium PBS pH 7,5 dengan koefisien regresi (R2 ) sebesar 0,9994 untuk puncak I dalam kisaran 0,06–5,0 μM dan untuk puncak II dalam kisaran 0,3–3,0 μM (Gambar 5D ). Selain itu, menggunakan grafik kalibrasi yang diperoleh dengan larutan DPT standar pada permukaan MWCNT/TiO2 / TiO2 / GCE, LOD dan LOQ untuk puncak I dan puncak II dihitung masing-masing sebesar 0,001 μM–0,005 μM dan 0,105 μM–0,351 μM.
Penentuan DPT dalam sampel tanah yang dicampur dengan berbagai konsentrasi diselidiki menggunakan elektroda termodifikasi MWCNT/TiO2 / TiO2 dengan AdSDPV (Gambar 5E ). Dalam medium PBS pH 7,5, arus puncak anoda menunjukkan korelasi linear dengan konsentrasi DPT dalam sampel tanah yang dicampur. Hubungan ini diamati dalam kisaran 0,2–5,0 μM untuk puncak I dan 0,5–5,0 μM untuk puncak II (Gambar 5F ). LOD dan LOQ juga dihitung sebagai 0,0175 dan 0,0583 μM untuk puncak I, 0,0208, dan 0,0695 μM untuk puncak II, masing-masing, menggunakan grafik kalibrasi yang diperoleh dengan sampel tanah yang dicampur DPT.
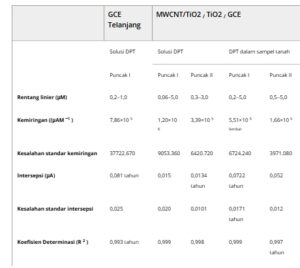
Data linearitas untuk menentukan DPT dalam larutan DPT standar dan sampel tanah yang dicampur pada konsentrasi berbeda dengan AdSDPV untuk elektroda yang tidak dimodifikasi dan dimodifikasi ditunjukkan pada Tabel 1 .
Tabel 1. Data regresi kurva kalibrasi untuk deteksi DPT.
[a] Semua nilai mewakili rata-rata tiga pengukuran.
2.7 Aplikasi Sensor yang Dikembangkan pada Sampel Lingkungan
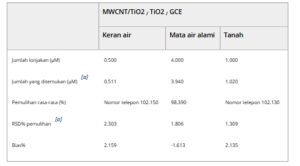
Teknik penambahan standar menilai penerapan dan akurasi sensor untuk menentukan DPT dalam sampel tanah, mata air alami, dan air ledeng. Grafik kalibrasi linier menentukan jumlah DPT dalam sampel tanah. Sebaliknya, persamaan linier yang diturunkan dari larutan standar menilai jumlah DPT dalam sampel air ledeng dan mata air alami. Selanjutnya, sejumlah larutan DPT standar yang diketahui ditambahkan ke sampel tanah, mata air alami, dan air ledeng. Pengukuran dilakukan dan dicatat dengan AdSDPV. Konsentrasi DPT dalam sampel yang ditambahkan ditentukan menggunakan persamaan kalibrasi, dan persentase pemulihan dihitung sebagai rasio jumlah yang ditambahkan dengan jumlah yang terdeteksi. Hasil analisis pemulihan (102,15%, 98,39%, dan 102,13%) menunjukkan efisiensi dan keandalan AdSDPV untuk menganalisis air ledeng, mata air alami, dan sampel tanah. Selanjutnya, deviasi standar relatif (RSD%) masing-masing adalah sekitar 2,30%, 1,81%, dan 1,31%, yang menunjukkan bahwa sensor MWCNT/TiO2 / TiO2 / GCE menunjukkan pengulangan yang baik (Tabel 2 ).
Tabel 2. Data yang diperoleh dari deteksi DPT dalam sampel tanah, mata air alami dan air keran.
[a] Nilai yang diberikan adalah rata-rata dari tiga pengukuran.
2.8 Investigasi Selektivitas Sensor yang Dikembangkan
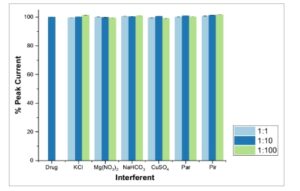
Untuk memeriksa selektivitas sensor yang dikembangkan, dampak senyawa organik seperti parasetamol (Par) dan pirfenidon (Pir) dan senyawa anorganik (CuSO 4 , KCl, NaHCO 3, dan Mg(NO 3 ) 2 ) yang dapat mengganggu penentuan DPT dalam sampel nyata (tanah, air) diselidiki pada GCE yang dimodifikasi dengan MWCNT/TiO 2 /TiO 2 dalam medium PBS pH 7,5. Larutan pengukuran yang mengandung berbagai senyawa pengganggu dan zat aktif DPT disiapkan dalam berbagai rasio (1 : 1, 1 : 10, 1 : 100). Konsentrasi DPT dijaga konstan pada 0,5 μM, dan pengukuran dilakukan dengan AdSDPV dengan mengubah konsentrasi zat pengganggu. % arus puncak ditentukan dengan menyandingkan puncak yang diamati dalam larutan standar DPT dengan sinyal yang terdeteksi dalam DPT yang mengandung campuran interferensi. Nilai ini berada di antara 99% dan 101% (Gambar 6 ). Hanya sedikit perubahan yang diamati pada sinyal oksidasi DPT. Hal ini membuktikan bahwa potensi gangguan dari bahan lain memiliki efek yang dapat diabaikan pada arus DPT.
Gambar 6
Buka di penampil gambar
Kekuatan Gambar
Diperoleh hasil menggunakan AdDPSV dengan elektroda MWCNT/TiO2 / TiO2 yang dimodifikasi untuk DPT 0,5 μM dengan adanya senyawa pengganggu yang berbeda.
Parameter validasi seperti sensitivitas, selektivitas, linearitas, dan akurasi dipelajari untuk menilai kinerja karbon kaca polos dan elektroda MWCNT/TiO2 / TiO2 / GCE untuk analisis DPT. Penentuan DPT yang lebih sensitif dilakukan dengan sensor yang dikembangkan dalam rentang linier yang lebih lebar daripada elektroda polos. Dapat dikatakan bahwa pembentukan dua sinyal, puncak I dan puncak II, dengan elektroda yang dimodifikasi, meningkatkan mekanisme transfer elektron dari sensor yang dikembangkan. Ketika nilai yang diperoleh dibandingkan dengan sensor lain yang dikembangkan untuk penentuan DPT dalam literatur, perbandingan dilakukan dengan nanosensor karena teknik kerja sensor MIP berbeda dari nanosensor (Tabel S1). Metode yang diusulkan mengungkapkan keefektifan sensor yang dikembangkan dengan memfasilitasi penentuan DPT pada nilai konsentrasi yang lebih rendah daripada yang dilaporkan dalam literatur. Pemulihan tinggi diperoleh dalam sampel lingkungan dengan studi pemulihan. Hasil ini menunjukkan penerapan sensor dan metode yang dikembangkan. Ketika literatur diperiksa, terlihat bahwa aplikasi analitis DPT dibuat dalam air mineral dan air ledeng. Tidak ada aplikasi yang dilakukan pada tanah dan air mata air alami. Oleh karena itu, di antara studi elektrokimia yang telah dilakukan sejauh ini, studi ini tampaknya menjadi yang pertama yang menentukan DPT pada berbagai sampel lingkungan.
3 Kesimpulan
Sensor MWCNT/TiO2 / TiO2 / GCE untuk daptomycin dikembangkan untuk pertama kalinya. Elektroda ini disiapkan menggunakan metode drop-dry. Teknik AdSDPV dan CV digunakan untuk penentuan DPT. Karakterisasi permukaan sensor MWCNT/TiO2 / TiO2 disinari dengan SEM, SEM-EDX. Studi linearitas dilakukan untuk kedua elektroda. Studi ini membuktikan bahwa LOD dan LOQ yang lebih rendah diperoleh daripada nilai yang dinyatakan dalam literatur. Sensor yang didukung diimplementasikan secara terpisah untuk mendeteksi daptomycin dalam sampel air dan tanah. Pemulihan yang tinggi diperoleh. Selektivitas metode dan sensor yang didukung diteliti terhadap senyawa organik dan anorganik. Selektivitas MWCNT/TiO2 / TiO2 / GCE dan teknik voltametri untuk deteksi daptomycin ditunjukkan dengan arus %peak.
Hasilnya, sensor generasi baru yang mudah diproduksi, selektif, sensitif, memiliki pemulihan tinggi, dan memiliki kesalahan relatif rendah diproduksi untuk pertama kalinya guna menentukan daptomycin dan diaplikasikan dalam berbagai sampel lingkungan. Sensor yang digunakan dalam penentuan elektrokimia DPT telah membawa inovasi ke dalam literatur karena belum pernah dipelajari sebelumnya dan belum diaplikasikan pada analisis sampel lingkungan (tanah, mata air alami, dan air ledeng) dengan metode elektroanalitik apa pun. Sensor ini menawarkan keuntungan dalam hal mudah disiapkan, murah, ramah lingkungan dan ramah pengguna, serta mudah diaplikasikan pada sampel lingkungan. Diharapkan bahwa sensor dan metode yang dikembangkan dapat dievaluasi dalam analisis rutin obat ini.





Tinggalkan Balasan